Contenu
- L'histoire
- Lois sur le dépistage néonatal
- Dépistage de base et secondaire
- Comment le dépistage est-il effectué
- Un mot de Verywell
Il existe actuellement aux États-Unis 35 troubles génétiques et métaboliques pour lesquels un dépistage est recommandé et 26 troubles secondaires pour lesquels un dépistage peut être effectué. La liste des tests de dépistage néonatal peut varier selon les États, la plupart en exécutant au moins 30.
L'histoire
Le concept de dépistage néonatal a commencé dans les années 1960 avec la mise au point d'un test de dépistage génétique de la phénylcétonurie, une anomalie métabolique congénitale. La méthode innovante et la collecte et le transport d'échantillons de sang sur papier filtre ont rendu le dépistage à grande échelle non seulement viable mais aussi coûteux. efficace.
Depuis lors, de nombreux autres tests de dépistage à base de sang ont été développés, y compris les nouvelles technologies de spectrométrie de masse en tandem (MS / MS) qui peuvent dépister plusieurs troubles en utilisant seulement quelques gouttes de sang séché.
Contrairement aux tests sanguins traditionnels qui doivent être évalués individuellement, la SEP / SEP peut détecter un large éventail d'anomalies congénitales à l'aide d'un appareil appelé spectromètre de masse, qui identifie les enzymes et les protéines en fonction des modèles de lumière réfractée. En comparant les résultats à une plage de référence de valeurs attendues, les techniciens de laboratoire peuvent confirmer avec une grande précision si un trouble génétique ou métabolique est présent, généralement en deux ou trois minutes.
En plus des tests sanguins, l'audition est régulièrement testée pour détecter la perte auditive du nouveau-né. Les tests auditifs sont non invasifs et ne prennent que quelques minutes à effectuer.
Aujourd'hui, plus de 98% des quatre millions de nouveau-nés nés chaque année aux États-Unis sont testés pour plus de 30 maladies génétiques, métaboliques, endocriniennes et infectieuses traitables au cours de la première semaine de vie.
Lois sur le dépistage néonatal
Le Comité consultatif sur les troubles héréditaires du nouveau-né et de l'enfant (ACHDNC) publie régulièrement des avis connus sous le nom de Panel de dépistage universel recommandé (RUSP) qui énumère les affections de base pour lesquelles le dépistage néonatal est fortement recommandé et les affections secondaires pour lesquelles le dépistage est facultatif.
Alors que les 50 États et le District de Columbia offrent le dépistage néonatal, il n'y a pas de loi fédérale régissant ce dépistage. Pour cette raison, les États peuvent choisir de changer le panel de troubles répertoriés dans le RUSP et / ou de transférer la responsabilité des tests de l'État au médecin ou à l'établissement individuel. Cela peut conduire à un manque important d'équité dans certains États.
En 2017, 49 États et le district de Columbia dépistaient au moins 30 des maladies de base recommandées par l'ACHDNC. D'autres États comme la Californie dépistaient plus que les 34 principaux et, ce faisant, réduisent considérablement leurs soins de santé annuels les coûts.
Le financement des programmes de dépistage continue de remettre en question de nombreuses législatures d'État. Pour remédier à cela, un projet de loi appelé Newborn Screening Saves Lives Reauthorization Act a été présenté à la Chambre des représentants des États-Unis en mai 2019 pour améliorer et étendre les initiatives actuelles de dépistage néonatal à travers les États-Unis.
Dépistage de base et secondaire
Depuis juillet 2018, il y a 35 conditions de base que l'ACHDNC recommande d'être inclus dans les dépistages de routine et 24 conditions secondaires qui doit être considéré en fonction de la disponibilité de traitements efficaces.
Conditions de base
Acidémie propionique
Acidémie méthylmalonique (méthylmalonyl-CoA mutase)
Acidémie méthylmalonique (troubles de la cobalamine)
Acidémie isovalérique
Déficit en 3-méthylcrotonyl-CoA carboxylase
Acidurie 3-hydroxy-3-méthylglutarique
Déficit en holocarboxylase synthase
Déficit en bêta-cétothiolase
Acidémie glutarique de type I
Absorption de carnitine / défaut de transport
Déficit en acyl-CoA déshydrogénase à chaîne moyenne
Déficit en acyl-CoA déshydrogénase à très longue chaîne
Déficit en L-3 hydroxyacyl-CoA déshydrogénase à longue chaîne
Déficit protéique trifonctionnel
Acidurie argininosuccinique
Citrullinémie, type I
Maladie de l'urine du sirop d'érable
Homocystinurie
Phénylcétonurie
Tyrosinémie, type I
Hypothyroïdie congénitale primaire
Hyperplasie surrénale congénitale
Anémie falciforme (maladie SS)
Bêta-thalassémie faucille
Anémie falciforme (maladie SC)
Déficit en biotinidase
Maladie cardiaque congénitale critique
Fibrose kystique
Galactosémie
Maladie du stockage du glycogène de type II
Perte auditive congénitale
Déficit immunitaire combiné sévère
Mucopolysaccharidose de type 1
Adrénoleucodystrophie liée à l'X
Atrophie musculaire spinale due à une délétion homozygote
Acidémie méthylmalonique avec homocystinurie
Acidémie malonique
Isobutyrylglycinurie
2-méthylbutyrylglycinurie
Acidurie 3-méthylglutaconique
Acidurie 2-méthyl-3-hydroxybutyrique
Déficit en acyl-CoA déshydrogénase à chaîne courte
Déficit en L-3-hydroxyacyl-CoA déshydrogénase à chaîne moyenne / courte
Acidémie glutarique de type II
Déficit en cétoacyl-CoA thiolase à chaîne moyenne
Déficit en 2,4 diénoyl-CoA réductase
Déficit en carnitine palmitoyltransférase de type I
Déficit en carnitine palmitoyltransférase de type II
Déficit en carnitine acylcarnitine translocase
Argininémie
Citrullinémie, type II
Hyperméthioninémie
Hyperphénylalaninémie bénigne
Défaut de bioptérine dans la biosynthèse des cofacteurs
Défaut de la bioptérine dans la régénération du cofacteur
Tyrosinémie de type II
Tyrosinémie de type III
Diverses autres hémoglobinopathies
Déficit en galactoépimérase
Déficit en galactokinase
Carences lymphocytaires liées aux lymphocytes T
Comment le dépistage est-il effectué
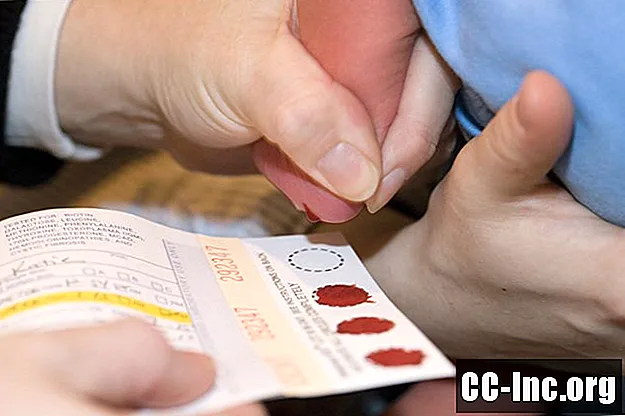
Le processus de dépistage néonatal est relativement rapide et facile. Entre 24 heures et 7 jours après la naissance, quelques gouttes de sang sont prélevées sur le talon d’un nourrisson et placées sur une carte spéciale. Le papier est envoyé à un laboratoire spécialisé pour être testé.
Les résultats des tests sanguins sont envoyés au pédiatre du nourrisson dans un délai de deux à sept jours. Si l'un des tests s'avère positif, d'autres tests seront effectués pour confirmer le diagnostic. Les parents n'ont pas à demander les tests; ils devraient être exécutés automatiquement.
En plus des tests sanguins, un test auditif sera effectué pour vérifier la perte d'audition. Il s'agit d'un test non invasif qui ne prend que cinq à dix minutes environ.
Il existe deux méthodes standard de détection de la perte auditive chez les nouveau-nés:
- Émissions otoacoustiques (OAE): Un écouteur et un microphone miniatures peuvent confirmer l'audition si les sons sont réfléchis par le conduit auditif.
- Réponse auditive du tronc cérébral (ABR): Les électrodes placées sur la tête du nouveau-né peuvent détecter la présence ou l’absence de réponse du cerveau aux sons.
Un mot de Verywell
Avec de nombreux troubles congénitaux, les symptômes ne deviendront apparents que quelques jours ou semaines après la naissance de l'enfant. En identifiant ces conditions tôt, un traitement peut être administré pour éviter d'endommager le cœur, les poumons, les reins, le système nerveux ou tout autre organe affecté.
Si vous avez des antécédents familiaux de trouble congénital, informez votre OB / GYN afin que des tests puissent être demandés s'ils ne sont pas déjà inclus dans le dépistage obligatoire.